Ny forskning skal vise, hvor meget proteiner mætter
Proteiner er gennem de senere år blevet utroligt populære som ingredienser i fødevarer – fx i syrnede mælkeprodukter. På den baggrund er et tværfagligt hold forskere i samarbejde med to virksomheder ved at undersøge, hvad struktur og forarbejdning af proteiner betyder for vores fysiologi – bl.a. hvordan vi fordøjer dem, hvor mætte vi bliver af dem, og hvordan vi omsætter energien fra dem.
De proteiner, der indgår som ingredienser i fødevarer, bliver typisk købt som færdige pulverprodukter, der allerede har gennemgået en processering. Men som det er i dag, ved man ikke særlig meget om, hvilken processering, der er bedst i forhold til anvendelsen. Forskerne i projektet StrucSat har en hypotese om, at forarbejdningen har stor betydning for, hvordan den færdige fødevare påvirker vores fysiologi – herunder, hvor mætte vi bliver af at spise produkterne, og hvordan vi optager energien fra dem.
”Vi har valgt at arbejde med et protein, der kommer fra ostevalle, beta-lakcoglobulin, samt et alginat, som er en kompleks sukkerart udtrukket fra tang. Alginat og protein udsætter vi for forskellige processer, både på proteinet for sig selv og for blandingen af protein og alginat for at se, hvordan de reagerer med hinanden,” siger leder af projektet, professor i food structure Richard Ipsen fra Institut for Fødevarevidenskab (FOOD) på Københavns Universitet, SCIENCE.

Professor Richard Ipsen. Foto: Lene Hundborg Koss
Testes i tre faser
Forskerne laver partikler, som er mere eller mindre tæt bundet sammen, og som bliver testet i proteinlaboratoriet på Institut for Fødevarevidenskab, hvor forskerne benytter sig af forenklede udgaver af den menneskelige fordøjelsesproces ved hjælp af reagensglas og enzymer fra maven og tarmen. De blandinger, som ser ud til at have den største effekt på vores fysiologi – enten fordi de er særligt svære eller særligt lette at nedbryde – går videre til forsøg på mus. Til sidst vil de mest lovende protein- og alginat-blandinger blive testet på mennesker.
”Vi skal til at starte på museforsøgene nu. Det, vi foreløbig har fundet ud af i laboratoriet, er, at proteinerne bliver dårligere fordøjet, hvis de er kraftigt opvarmet. Grundlæggende tror vi på, man opnår en bedre mæthed, hvis vi kan forsinke nedbrydningen af proteinerne, til de er kommet et godt stykke ned i tarmsystemet,” siger professor Richard Ipsen.
Hurtigt eller langsomt mæt
Med resultaterne fra projektet håber forskerne at kunne fortælle fødevareindustrien, hvilke behandlinger proteiner skal have for at egne sig bedst til de forskellige færdige fødevarer. Vil man fx lave en proteindrik til ældre, der har svært ved at indtage store mængder, skal forarbejdningen tage højde for dette – tilsvarende hvis man laver produkter, der skal mætte ved et lavt indtag af kalorier.
Partnere i StrucSat
Virksomheder: Arla Foods Ingredient Group R&D, DK; DuPont Nutrition and Health
Universiteter og forskningsinstitutioner: DTU; IFR (Institute of Food Research), UK; NIFES (Nasjonalt institutt for ernærings- og sjømatforskning), Norge
Fra Københavns Universitet deltager følgende institutter: Biologisk Institut (BIO); Institut for Idræt og Ernæring (NEXS); Institut for Fødevarevidenskab (FOOD), som leder projektet
StrucSat er finansieret af Det Strategiske Forskningsråd, der har støttet projektet med over 17 millioner kroner.
Emner
Relaterede nyheder
Atomic force mikroskopi fotos
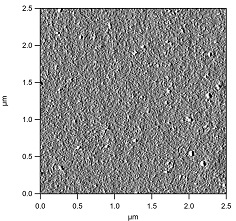

Atomic force mikroskopi (AFM) billeder af serum protein koncentrat (SPC) prøver ved pH: 6,0, opnået ved ikke-opvarmede forhold (øverste billede) og efter varmebehandling ved 85 graders celcius i 10 minutter (nederste billede). Den ikke-opvarmede prøve havde meget små partikler med rund form og fordelingen af partiklerne var homogen (øverste billede). Den opvarmede prøve havde partikler med forskellige størrelser og former og fordelingen af partiklerne var heterogen (nederste billede). De forskellige test-strukturer (partikelstørrelse, form og distribution), kan have en stor indflydelse på fordøjelsesenzymernes modtagelighed over for dem, og fx på øget mæthed, der kan mindske indtagelse af fødevarer.
